Data: 07/05/2021 – Iniciativa do GEDIIB através do comitê Covid-19
O Grupo de Estudos de Doença Inflamatória Intestinal do Brasil (GEDIIB), atento às novas evidências relacionadas à COVID-19, atualizou o posicionamento sobre a vacinação para SARS-CoV2 em pacientes com DII.
A pandemia de COVID-19 é uma emergência de saúde pública de interesse internacional e o Brasil é atualmente uma das regiões mais atingidas, tendo uma das maiores taxas de mortalidade de COVID-19 do mundo [1]. A vacinação em massa oferece a melhor estratégia para enfrentamento da pandemia de COVID-19, e as vacinas contra SARS-CoV2 foram aprovadas em vários países para uso emergencial. No Brasil, desde a sua aprovação, o maior desafio tem sido garantir a vacinação em massa num menor intervalo de tempo possível. Existem potenciais preocupações em relação às recomendações de vacinas para populações específicas, como pacientes com doença inflamatória intestinal (DII), especialmente aqueles que recebem terapia imunossupressora. Para responder a essas questões, o Grupo de Estudos de Doença Inflamatória Intestinal do Brasil (GEDIIB), fornece conselhos práticos com recomendações importantes sobre as vacinas para COVID-19 na população com DII e os atualiza periodicamente, de acordo com as novas informações disponíveis.
I. Os pacientes com DII devem ser priorizados nos grupos de distribuição de vacinação?
Dados recentes sugerem que pacientes com DII não têm um risco aumentado de infecção de SARS-CoV2 ou de desenvolvimento de complicações COVID-19 [2]. Portanto, é improvável que um paciente com DII se qualifique para um grupo prioritário de vacinação com base isoladamente no diagnóstico de DII. Entretanto, os pacientes com DII geralmente requerem tratamento com medicamentos imunossupressores, que podem aumentar o risco de infecções. Neste contexto, recentemente o programa nacional de imunização (PNI) incluiu pacientes em uso de imunossupressores como grupo prioritário para a vacinação contra a COVID-19. Definimos como indivíduos portadores de DII em terapia imunossupressora aqueles em uso de:
- Dose de prednisona > 10 mg/dia ou equivalente;
- Imunossupressores (azatioprina ou metotrexato);
- Imunobiológicos (anti-TNF, anti-interginas ou anti-interleucinas)
- Pequenas moléculas (Tofacitinibe)
II. Como os pacientes devem comprovar a terapia imunossupressora?
A exigência da documentação comprobatória será definida pelos órgãos regulatórios de cada região. Prescritores e pacientes deverão seguir as recomendações locais.
III. Quais vacinas estão disponíveis atualmente?
As primeiras imunizações aprovadas pelas agências reguladoras europeias e americanas foram as vacinas de RNAm. No Brasil, a nossa agência reguladora autorizou o uso emergencial para as vacinas Oxford/AstraZeneca e Sinovac SARS-CoV-2. A Tabela 1 fornece uma visão geral das principais vacinas para SARS-CoV2.
Tabela 1 – Visão geral das vacinas SARS-CoV-2 aprovadas
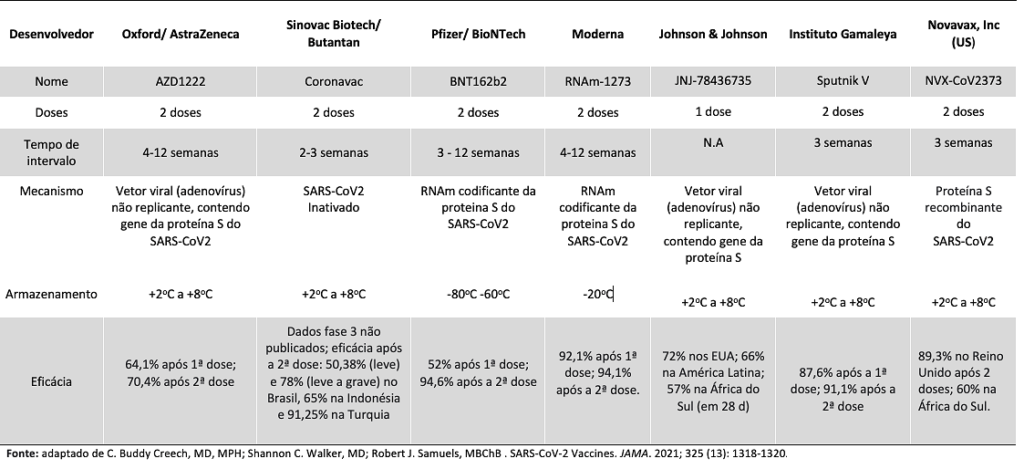
Clique AQUI para ver a tabela ampliada
III. A imunossupressão afeta a eficácia da vacina COVID-19?
Para outras vacinas comuns, foi demonstrado que medicamentos imunossupressores podem resultar em alguma redução na formação de anticorpos e menor resposta vacinal. Por exemplo, foi demonstrado que a resposta imune à vacinação pneumocócica polissacarídica (PSV-23) é prejudicada em pacientes com doença de Crohn (CD) em terapia combinada de biológicos anti-TNF e imunomoduladores [3], também é afetada a taxa de conversão sorológica para vacina contra influenza em pacientes imunossuprimidos com DII [4,5]. Por outro lado, o tratamento com ustequinumabe ou vedolizumabe não parecem reduzir as respostas à vacina contra a gripe [6,7]. Não sabemos se as vacinas disponíveis são tão eficazes em pacientes com DII, visto que a maioria dos ensaios de vacinas excluiu os pacientes com este diagnóstico. Levando em consideração o maior nível de eficácia das vacinas disponíveis contra COVID-19 sintomático e COVID-19 grave (70% -95%), muito melhor do que a vacina contra gripe (50%-60%), prevê-se que a vacina para SARS COV-2 proteja em taxas mais altas, mesmo que o tratamento com agentes imunossupressores possa interferir na resposta.
IV. Há alguma preocupação de segurança em relação à vacinação contra SARS-Cov-2 em pacientes com DII?
Não há evidências que sugiram um risco aumentado das vacinas contra SARS-CoV-2 em pacientes com DII. Embora seja possível que outras vacinas estejam disponíveis em breve, é importante ressaltar que, para as listadas na Tabela 1, a imunossupressão não é uma contra-indicação. Além disso, as vacinas SARS-CoV2 foram testadas em dezenas de milhares de pacientes com perfis de segurança muito semelhantes a outras vacinas comumente usadas em pacientes com DII, como a vacina contra a gripe. Adicionalmente, os pacientes com DII foram vacinados com vacinas contra influenza e pneumonia por muitos anos, sem indicação de agravamento dos sintomas de DII ou exacerbações após a vacinação [4]. Assim, semelhante a outras vacinas usadas por muitos anos, a imunização parece muito improvável de afetar a atividade da DII.
Recentemente foi descrita uma possível associação entre a vacina Oxford/Astrazeneca e eventos tromboembólicos com trombocitopenia, o que representaria uma preocupação, especialmente nos portadores de DII em atividade. Entretanto, a frequência destes eventos foi classificada como muito rara: na Europa foram relatados 30 casos entre aproximadamente 5 milhões de doses aplicadas, e a frequência de tromboembolismo na população vacinada não foi superior àquela observada na população em geral [8]. No Brasil, até o momento, foram registrados 47 casos suspeitos entre cerca de 4 milhões de doses administradas da vacina. A agência regulatória nacional recentemente determinou que houvesse a inclusão desta informação na bula da vacina, porém esclarece que os benefícios do uso da vacina Oxford/Astrazeneca superam muito os potenciais riscos e manteve a recomendação da sua administração [9].
V. Os pacientes com DII devem adiar o tratamento biológico ou suspender a imunossupressão para serem vacinados?
Recomendamos que a vacina COVID-19 seja administrada a qualquer momento, independentemente da última infusão biológica/dose subcutânea recebida, pois nenhuma das vacinas contém o coronavírus vivo e os vetores virais utilizados em algumas vacinas (adenovírus) não é capaz de causar infecção em humanos. A única recomendação a esse respeito é que os pacientes devem evitar receber a vacina no mesmo dia da infusão/dose subcutânea, pois, caso o mesmo desenvolva alguma reação ou evento adverso, seria difícil identificar qual agente (vacina ou biológico) causador a reação.
Portanto, à luz das evidências atuais, apoiamos fortemente a recomendação de vacinar todos os pacientes com DII contra a SARS-CoV2, independentemente do seu tratamento atual. Para situações específicas não discutidas neste documento, recomendamos que a decisão de vacinar ou não seja tomada individualmente, a partir de uma decisão compartilhada entre pacientes e médicos.
Esta revisão representa a opinião de um grupo de especialistas e do GEDIIB. Está de acordo com as evidências disponíveis e o posicionamento dos principais grupos internacionais de especialistas em DII. Outras vacinas poderão ser aprovadas e novos dados disponibilizados em poucas semanas. Portanto, esta recomendação pode mudar e será revisada periodicamente, com posterior publicação no site do GEDIIB
Referências
1. Dong E, Du H, Gardner L. An interactive web-based dashboard to track COVID-19 in real time. Lancet Infect Dis 2020;20(5):533–4.
2. Brenner EJ, Ungaro RC, Gearry RB, Kaplan GG, Kissous-Hunt M, Lewis JD, et al. Corticosteroids, but not TNF Antagonists, are Associated with Adverse COVID-19 Outcomes in Patients With Inflammatory Bowel Diseases: Results from an International Registry. Gastroenterology 2020.
3. Melmed GY, Agarwal N, Frenck RW, Ippoliti AF, Ibanez P, Papadakis KA, et al. Immunosuppression impairs response to pneumococcal polysaccharide vaccination in patients with inflammatory bowel disease. Am J Gastroenterol 2010;105(1):148–54.
4. Mamula P, Markowitz JE, Piccoli DA, Klimov A, Cohen L, Baldassano RN. Immune response to influenza vaccine in pediatric patients with inflammatory bowel disease. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc 2007;5(7):851–6.
5. Cullen G, Bader C, Korzenik JR, Sands BE. Serological response to the 2009 H1N1 influenza vaccination in patients with inflammatory bowel disease. Gut 2012;61(3):385–91.
6. Caldera F, Hillman L, Saha S, Wald A, Grimes I, Zhang Y, et al. Immunogenicity of High Dose Influenza Vaccine for Patients with Inflammatory Bowel Disease on Anti-TNF Monotherapy: A Randomized Clinical Trial. Inflamm Bowel Dis 2020;26(4):593–602.
7. Doornekamp L, Goetgebuer RL, Schmitz KS, Goeijenbier M, van der Woude CJ, Fouchier R, et al. High Immunogenicity to Influenza Vaccination in Crohn’s Disease Patients Treated with Ustekinumab. Vaccines 2020;8(3).
8. Søren Dinesen Østergaard, Morten Schmidt, Erzsébet Horváth-Puhó, Reimar Wernich Thomsen, Henrik Toft Sørensen. Thromboembolism and the Oxford–AstraZeneca COVID-19 vaccine: side- effect or coincidence? Lancet 2021;397(10283):1441-1443
9. Disponível em: https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2021/anvisa-solicita-alteracao-de-bula-da-vacina-de-oxford/comunicado_ggmon_004_2021.pdf.
Comments are closed.
 +55 11 9.4580-5406
+55 11 9.4580-5406
